近日,国家药监局批准诺辉健康旗下产品常卫清的创新三类医疗器械注册申请,诺辉健康方面称,
该产品适用于年龄40-74岁的结直肠癌高风险人群,不能替代肠镜,不能用于普通人群的肿瘤筛查,临床诊断过程中不应以本产品检验测试结果作为临床诊断的唯一依据。
11月21日消息,国家药品监督管理局应急审批通过了丰台区医疗器械生产企业北京金沃夫生物工程科技有限公司申报的新冠病毒(2019-nCoV)抗原检测试剂盒(乳胶法)产品。上述产品是我国首次批准新冠病毒抗原检测试剂之一。
丰台区市场监督管理局多措并举助力企业最终取得首批新冠病毒(2019-nCoV)抗原检测试剂盒产品注册证。
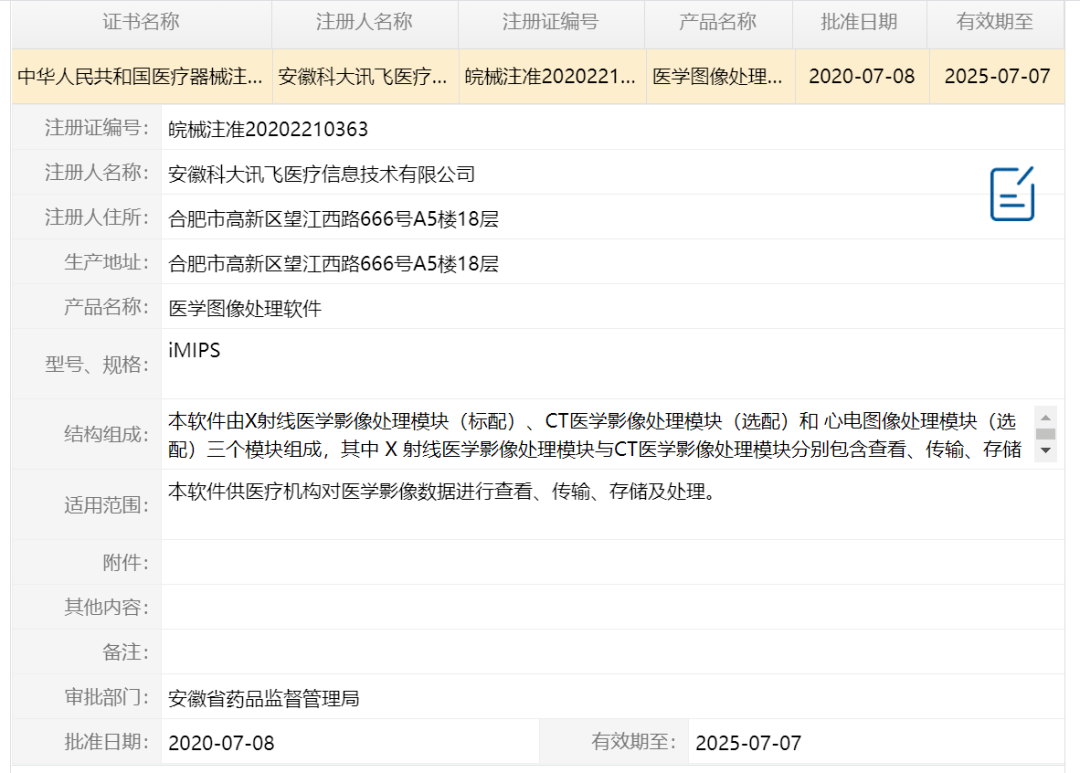
11月4日消息,科大讯飞成功获得二类医疗器械注册证及ISO13485体系认证。
此次拿证,是科大讯飞在疫情风口下的一大突破。为疫情防控工作取得突破,科大讯飞3天内便快速实现新冠肺炎影像辅助诊断系统现场部署落地应用,并通过数据迭代与算法优化保证系统每日升级。
相较于传统阅片工具,新冠肺炎影像辅助诊断系统提供的4D对比分析功能,可以在一定程度上完成多期影像中的病灶数量、病灶体积变化、病灶密度变化等量化对比分析功能,使影像科医生快速掌握病灶变化,大幅度提高医生分析患者病情变化的效率。
据悉,此次进入创新医疗器械特别审批程序的“骨科手术导航定位系统TiRobot Recon”是一款全膝关节置换手术机器人。TiRobot Recon辅助外科医生进行全膝关节置换手术,系统辅助医生完成基于患者解剖和运动学的个体化关节置换手术设计,并完成定位膝关节假体安装需要的截骨定位。目前国内尚无同种类型的产品上市。
作为全球医疗器械巨头,美敦力已连续参加三届进博会。脊柱Mazor X StealthTM Editio外科手术机器人,系在国内的首次公开亮相。
此次亮相的Mazor X StealthTM Edition脊柱外科手术定位与导航系统便是标志性产品,美敦力智能手术生态系统的核心节点,它的出现,意味着全球脊柱手术机器人行业的标准将被重塑。
“脊柱外科手术定位与导航系统”听上去很复杂,简单来说就是将美敦力的Stealth平台与Mazor现有的机器人技术相结合,再加上智能算法,实现手术的术前规划和手术的执行,为脊柱外科医生提供精确的手术入路引导和可视化信息,满足“高精密度和准确度”的手术目标。据了解,Mazor X StealthTM Edition目前已进入注册流程,有望于明年在国内上市。
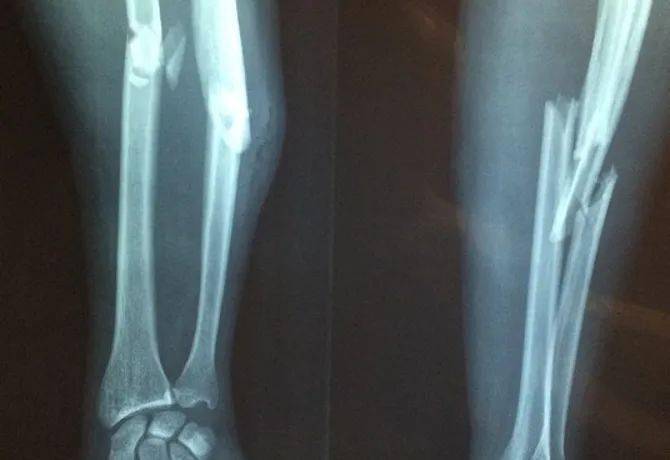
11月14日消息,联影智能近日宣布公司获得全球首张CT骨折医疗AI三类证。
此次获批的CT骨折智能分析系统具备“精准肋骨定位,秒级骨折检出,直观提示病灶”等一系列特点,以高敏感性辅助医生快速、高效、精准地完成肋骨的诊断,避免错诊和漏诊。
11月13日消息,国家药品监督管理局(NMPA)正式批准推想医疗科技股份有限公司(简称推想科技)的肺结节AI三类认证,这也是国家药品监督管理局批准的第一张肺部AI三类认证。
今年初,推想科技以全球第一家的身份,拿到了胸肺CT领域AI的FDA和PMDA认证。至此,推想科技也成为全世界唯一一个拥有中国NMPA、欧盟CE、日本PMDA、美国FDA四大认证的AI医疗公司,获得了全球多个主要医疗市场的准入资格。
自今年2月以来,推想科技陆续获得欧盟CE认证、日本PMDA认证、美国FDA认证,并第一个拿到最具含金量的首个中国肺部AI三类认证。此外,推想AI也是FDA批准的第一款肺部CT深度学习产品。四张准入认证不仅覆盖了中国、美国、欧盟、日本这四个全球最主要的、医疗水平最高、准入审核最严格的市场,也为世界其他几个国家和地区的市场准入提供了重要参考。
这款新冠病毒(2019-nCoV)抗原检测试剂盒(胶体金法)检测时间在20分钟之内。在急性感染期病毒载量较高时能快速检出阳性病例,可用于对疑似人群进行早期分流和快速管理。
11月2日,广东省药监局发布《广东省医疗器械注册人试点品种清单》,华为终端有限公司腕部单导心电采集器(VID-B99)通过注册人申请进入清单。
通过查询国家药监局医械产品注册信息来看,该产品由主机、腕带、充电线、无线充电底座及移动端软件组成,用于成人腕部单导心电数据的采集,属于第二类医疗器械,受托人为歌尔股份有限公司。
近年来华为的身影一直活跃在医疗健康市场上。在医疗器械领域,华为不断将医疗器械纳入公司营业范围,为开展医械业务做铺垫。
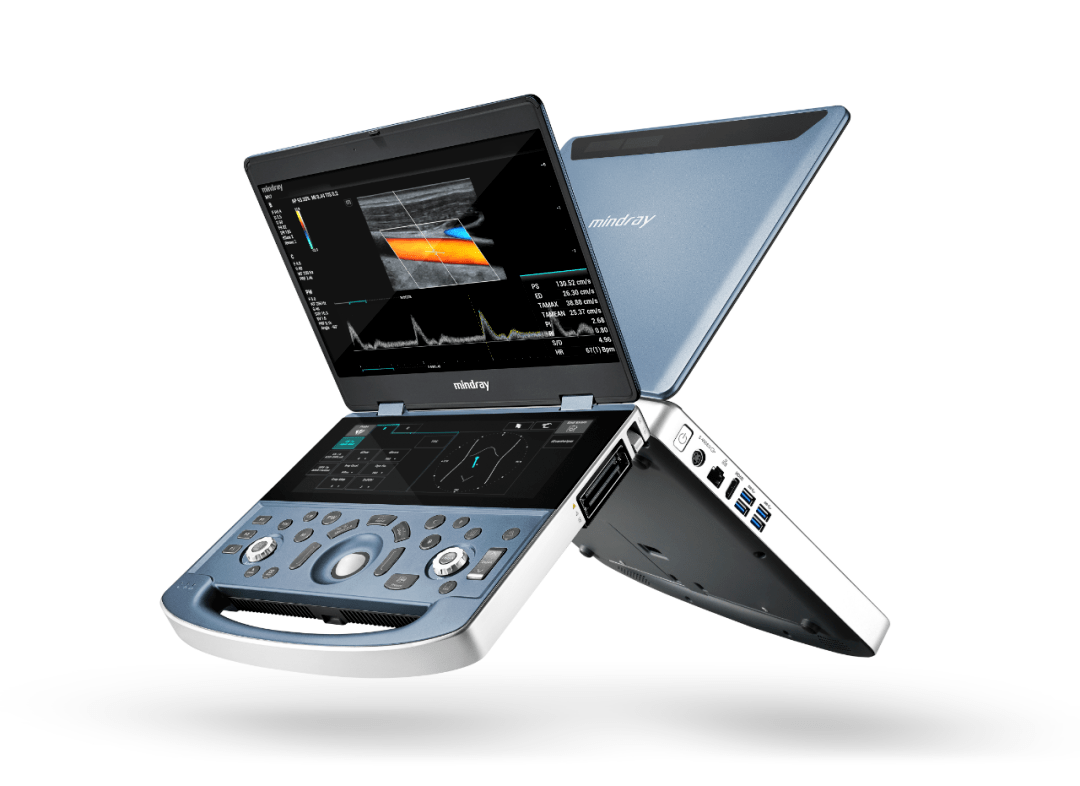
5个月,3轮评选,2轮答辩,最终从3.4万件参赛作品中脱颖而出——这是迈瑞MX系列斩获广东省第十届“省长杯”工业设计大赛最高荣誉钻石奖的历程。
迈瑞全新便携超声MX系列,基于前沿的域光平台,以仅重3kg、薄44mm的轻量化设计与8小时的超长续航等创新点树立了行业标杆。






米乐体育官方直播网站入口公众号
米乐体育官方直播网站公众号
联系我们
